Dermatologia e immunologia cutanea
Immunità e infiammazione di tipo 1, 2 e 3
Inquadramento concettuale e rilevanza dermatologica
Nei lavori scientifici i termini immunità di tipo 1, 2 e 3 e infiammazione di tipo 1, 2 e 3 vengono spesso usati in modo ravvicinato, talvolta quasi come sinonimi. In realtà indicano due livelli diversi dello stesso fenomeno biologico: il primo descrive l’architettura immunologica della risposta, il secondo il fenotipo infiammatorio che ne deriva nei tessuti.
Immunità e infiammazione: due piani concettuali diversi
La classificazione in risposte di tipo 1, tipo 2 e tipo 3 nasce dallo studio dei linfociti T helper e delle rispettive citochine effettrici. Con il tempo, però, questo modello si è ampliato: oggi non riguarda più soltanto i linfociti T, ma comprende anche cellule dell’immunità innata, cellule linfoidi innate, cheratinociti, cellule dendritiche, microbiota e segnali prodotti dalla barriera epiteliale.
Quando si parla di immunità di tipo 1, 2 o 3 ci si riferisce soprattutto ai circuiti cellulari e molecolari che organizzano la risposta: quali cellule sono attivate, quali citochine producono, quale tipo di patogeno o stimolo sono deputate a controllare. Quando invece si parla di infiammazione di tipo 1, 2 o 3, il punto di osservazione si sposta sul tessuto: quale pattern infiammatorio si manifesta, quali mediatori dominano, quali cellule vengono reclutate e quali conseguenze cliniche si osservano.
Punto chiave
L’immunità descrive il “programma” della risposta; l’infiammazione descrive il suo “risultato” clinico e tissutale. Per questo nei paper più recenti, soprattutto quando si parla di biologici, si preferisce spesso il linguaggio dei pattern infiammatori: è più vicino alla scelta terapeutica.
Risposta di tipo 1: immunità citotossica e asse IFN-γ
L’immunità di tipo 1 è il braccio della risposta immune più adatto al controllo dei patogeni intracellulari, come virus e micobatteri. È dominata dall’asse Th1, dalla produzione di interferone-γ (IFN-γ) e dall’attivazione di linfociti T citotossici, cellule NK e macrofagi polarizzati in senso pro-infiammatorio.
A livello cutaneo, quando questo programma diventa eccessivo o maldiretto, il risultato è un’infiammazione prevalentemente citotossica. Il bersaglio non è più soltanto il patogeno, ma può diventare una componente della cute stessa. In dermatologia questo modello aiuta a interpretare malattie come il lichen planus e la vitiligine, nelle quali il danno cellulare diretto ha un ruolo centrale.
Nel lichen planus la risposta citotossica contro i cheratinociti basali produce il tipico danno dell’interfaccia dermo-epidermica. Nella vitiligine, invece, l’asse IFN-γ/CXCL10 e i linfociti CD8+ sono implicati nella distruzione selettiva dei melanociti. In entrambi i casi il concetto di infiammazione di tipo 1 è più utile della semplice etichetta diagnostica, perché orienta il ragionamento verso pathway intracellulari e segnali interferonici.
Risposta di tipo 2: barriera, prurito e asse IL-4/IL-13
L’immunità di tipo 2 è fisiologicamente legata alla difesa contro elminti e parassiti, ma anche alle risposte allergiche e alla regolazione della barriera epiteliale. Le citochine chiave sono IL-4, IL-5 e IL-13; le cellule coinvolte includono linfociti Th2, eosinofili, mastociti, basofili e cellule linfoidi innate di tipo 2.
Nel linguaggio clinico, infiammazione di tipo 2 non significa necessariamente “risposta Th2 pura”. Il termine indica piuttosto un ambiente dominato dall’asse IL-4/IL-13, spesso accompagnato da prurito, alterazione di barriera, tendenza eczematosa, IgE elevate o eosinofilia, anche se questi elementi non sono sempre tutti presenti.
La dermatite atopica rappresenta il paradigma dermatologico più chiaro dell’infiammazione di tipo 2. In questa malattia il difetto di barriera e la risposta immunitaria si alimentano reciprocamente: la barriera alterata facilita l’ingresso di allergeni e irritanti, mentre le citochine di tipo 2 peggiorano ulteriormente la differenziazione epidermica e amplificano il prurito. Anche l’orticaria cronica spontanea può presentare componenti di tipo 2, sebbene la sua patogenesi sia più eterogenea e non riducibile a un unico asse.
Risposta di tipo 3: neutrofili, cheratinociti e asse IL-17/IL-23
L’immunità di tipo 3 è centrata sull’asse Th17/Th22 e sulla produzione di IL-17, IL-22 e, a monte, IL-23. È una risposta fondamentale contro batteri extracellulari e funghi, perché favorisce il reclutamento neutrofilico e potenzia le difese epiteliali.
Quando questo programma si attiva in modo patologico nella cute, l’infiammazione assume un profilo neutrofilico e iperproliferativo. I cheratinociti non sono semplici spettatori: rispondono a IL-17 e IL-22 producendo chemochine, peptidi antimicrobici e mediatori che mantengono il circuito infiammatorio. Il risultato clinico è spesso una cute ispessita, ipercheratosica, eritemato-squamosa.
La psoriasi è il modello più netto di infiammazione di tipo 3 in dermatologia. L’efficacia degli anti-IL-17 e degli anti-IL-23 ha reso particolarmente evidente quanto questo asse sia centrale nella malattia. Il successo terapeutico dei farmaci biologici, in questo caso, è anche una conferma clinica della correttezza del modello patogenetico.
Malattie ibride: quando un solo asse non basta
La tripartizione tipo 1, tipo 2 e tipo 3 è molto utile sul piano didattico, ma non deve essere interpretata in modo rigido. Molte dermatosi reali sono ibride: possono avere un asse dominante, ma anche componenti secondarie che cambiano nel tempo, variano tra pazienti diversi o diventano più evidenti in alcune fasi della malattia.
Il pemfigo volgare, ad esempio, è primariamente una malattia autoanticorpale e non rientra perfettamente nello schema tipo 1/2/3. Tuttavia presenta diversi elementi di polarizzazione di tipo 2, tra cui la produzione di autoanticorpi IgG4 e un ambiente citochinico compatibile con risposte Th2. Il lupus eritematoso cutaneo è fortemente condizionato da segnali interferonici e quindi da una componente di tipo 1, ma si inserisce in una rete immunologica molto più complessa. L’idrosadenite suppurativa, infine, mostra aspetti di tipo 1 e tipo 3, con una marcata eterogeneità clinica e terapeutica.
Ricaduta pratica
Ragionare per pathway non significa abbandonare la diagnosi clinica. Significa aggiungere un secondo livello: dopo aver dato un nome alla malattia, ci si chiede quale pattern infiammatorio sia dominante in quel paziente e in quella fase.
Perché questa distinzione è utile in terapia
La dermatologia contemporanea si sta spostando da una logica puramente nosografica a una logica sempre più molecolare. In passato due pazienti con la stessa diagnosi venivano spesso trattati nello stesso modo; oggi, almeno per alcune patologie, la scelta terapeutica dipende sempre più dal pathway dominante, dalla gravità, dalle comorbidità e dal profilo di sicurezza del farmaco.
Questo non significa che ogni dermatosi possa essere ridotta a una citochina. Al contrario, il valore del modello tipo 1/2/3 sta proprio nel rendere visibile la complessità, senza perdersi in essa. La diagnosi resta il punto di partenza, ma il pattern infiammatorio aiuta a comprendere perché un paziente risponde a un biologico, perché un altro non risponde, e perché alcune malattie cambiano aspetto clinico nel corso del tempo.
Tabella riassuntiva
| Tipo | Citochine chiave | Cellule prevalenti | Pattern clinico | Esempi dermatologici | Target terapeutici |
|---|---|---|---|---|---|
| Tipo 1 | IFN-γ, IL-2; segnali interferonici | Th1, CD8+, NK, macrofagi M1 | Citotossico, autoimmune, danno dell’interfaccia | Lichen planus, vitiligine, alcune forme di lupus cutaneo | JAK-inibitori, immunosoppressori, strategie anti-interferoniche in contesti selezionati |
| Tipo 2 | IL-4, IL-5, IL-13 | Th2, ILC2, eosinofili, mastociti, basofili | Pruriginoso, eczematoso, allergico, barriera-dipendente | Dermatite atopica, prurigo nodularis, orticaria cronica con componente type 2 | Anti-IL-4/IL-13, anti-IL-13, anti-IgE, anti-IL-5 in ambiti selezionati |
| Tipo 3 | IL-17A/F, IL-22, IL-23 | Th17, Th22, ILC3, neutrofili, cheratinociti attivati | Neutrofilico, iperproliferativo, eritemato-squamoso | Psoriasi, pustolosi, componenti di idrosadenite suppurativa | Anti-IL-17, anti-IL-23, anti-IL-12/23 |
| Ibrido | Variabili secondo malattia e fase clinica | Popolazioni miste | Fenotipo composito, spesso dinamico | Pemfigo volgare, lupus eritematoso cutaneo, idrosadenite suppurativa | Target multipli; scelta guidata da diagnosi, fenotipo e comorbidità |
Take-home message
Immunità e infiammazione di tipo 1, 2 e 3 non sono sinonimi perfetti. L’immunità indica il programma cellulare e molecolare; l’infiammazione indica il fenotipo biologico osservabile nel tessuto. In dermatologia questa distinzione è particolarmente utile perché collega la patogenesi alla terapia: non si cura soltanto una diagnosi, ma anche il pathway dominante che sostiene quella diagnosi in quel paziente.
Oltre il modello tipo 1–2–3: l’asse autoinfiammatorio
Sebbene la classificazione dell’infiammazione in tipo 1, tipo 2 e tipo 3 sia estremamente utile, essa non esaurisce la complessità delle risposte immunitarie osservate nella pratica clinica. In particolare, questo schema nasce storicamente dallo studio dell’immunità adattativa e delle cellule T helper, e descrive in modo ottimale condizioni in cui tali circuiti sono predominanti.
Esiste tuttavia un gruppo di patologie in cui la risposta immunitaria è guidata prevalentemente dall’immunità innata: le malattie autoinfiammatorie. In queste condizioni non vi è una risposta antigen-specifica dominante né la produzione di autoanticorpi patogenetici; il driver principale è invece l’attivazione aberrante dei sistemi di riconoscimento innati.
Il fulcro di queste malattie è rappresentato dall’inflammasoma, un complesso intracellulare che, in risposta a segnali di pericolo, promuove la produzione di citochine proinfiammatorie, in particolare interleuchina-1β (IL-1β) e interleuchina-18 (IL-18). Questo asse IL-1–centrico rappresenta il principale motore del danno tissutale.
Esempi paradigmatici sono la febbre mediterranea familiare e le sindromi CAPS, mentre in dermatologia manifestazioni autoinfiammatorie possono essere osservate anche in condizioni come la sindrome di Sweet e il pioderma gangrenoso, accomunate da un marcato infiltrato neutrofilico e da una forte attivazione dell’immunità innata.
Dal punto di vista patogenetico, queste condizioni non si collocano in modo diretto all’interno della classificazione tipo 1–2–3. Sebbene possano condividere alcune caratteristiche fenotipiche con l’infiammazione di tipo 3, in particolare la presenza di neutrofili, il meccanismo molecolare è profondamente diverso.
Punto chiave
Neutrofilico non significa automaticamente tipo 3. L’infiammazione di tipo 3 è mediata dall’asse IL-23/IL-17, mentre le condizioni autoinfiammatorie sono guidate principalmente dall’asse IL-1 e dall’attivazione dell’inflammasoma.
| Caratteristica | Infiammazione tipo 3 | Asse autoinfiammatorio |
|---|---|---|
| Citochine chiave | IL-17, IL-22, IL-23 | IL-1β, IL-18 |
| Cellule driver | Th17, ILC3 | Immunità innata (neutrofili, monociti, macrofagi) |
| Meccanismo centrale | Attivazione asse IL-23 → Th17 → IL-17 | Attivazione inflammasoma |
| Tipo di risposta | Adattativa (con contributo innato) | Innato puro |
| Pattern istologico | Neutrofilico + iperproliferazione epidermica | Neutrofilico puro |
| Esempi clinici | Psoriasi | Sindrome di Sweet, pioderma gangrenoso |
| Target terapeutici | Anti-IL-17, anti-IL-23 | Anti-IL-1 (anakinra, canakinumab) |
Questa distinzione ha implicazioni cliniche rilevanti. Le malattie caratterizzate da infiammazione di tipo 3 rispondono in modo ottimale a farmaci diretti contro IL-17 o IL-23, mentre le condizioni autoinfiammatorie mostrano una risposta marcata a farmaci che bloccano l’asse IL-1, come anakinra o canakinumab.
Accanto agli assi tipo 1, tipo 2 e tipo 3, è quindi utile considerare un quarto asse funzionale, definibile come asse autoinfiammatorio. L’integrazione di questo livello nel modello interpretativo consente una lettura più completa delle dermatosi infiammatorie e riflette l’evoluzione della dermatologia verso una classificazione basata sui meccanismi patogenetici.
La classificazione di Coombs e Gell: dove si colloca?
La storica classificazione di Coombs e Gell rappresenta ancora oggi uno dei pilastri concettuali dell’immunopatologia. Tuttavia, il suo obiettivo è diverso rispetto ai moderni modelli basati sugli assi tipo 1, tipo 2 e tipo 3.
La classificazione di Coombs e Gell descrive infatti il meccanismo effettore del danno immunologico: anticorpi, immunocomplessi o cellule T responsabili della lesione tissutale. I moderni pattern immunologici descrivono invece il programma immunitario dominante, cioè quali citochine, pathway e circuiti cellulari sostengano la malattia.
Punto chiave
Le due classificazioni non sono concorrenti, ma complementari. Coombs e Gell spiegano “come” avviene il danno; i pattern tipo 1–2–3 spiegano “quale circuito immunitario” guida la risposta.
| Malattia | Coombs-Gell | Pattern moderno dominante |
|---|---|---|
| Dermatite atopica | Tipo I (IgE-mediata) | Infiammazione di tipo 2 |
| Psoriasi | Tipo IV (cellulo-mediata) | Infiammazione di tipo 3 |
| Pemfigo volgare | Tipo II (autoanticorpi) | Pattern tipo 2 / B-cell driven |
| Dermatite allergica da contatto | Tipo IV | Tipo 1 / 17 variabile |
| Lupus eritematoso cutaneo | Tipo III (immunocomplessi) | Tipo 1 / interferonico |
Questa distinzione aiuta a comprendere l’evoluzione storica dell’immunologia clinica. Le classificazioni tradizionali erano centrate soprattutto su anticorpi, immunocomplessi e linfociti T; i modelli più recenti integrano invece citochine, immunità innata, inflammasoma, neuroimmunologia e pathway intracellulari.
In dermatologia, l’integrazione tra questi due livelli interpretativi è particolarmente utile: la classificazione di Coombs e Gell mantiene valore sul piano immunopatologico, mentre i pattern tipo 1–2–3 aiutano a interpretare il fenotipo clinico e a orientare la scelta terapeutica.
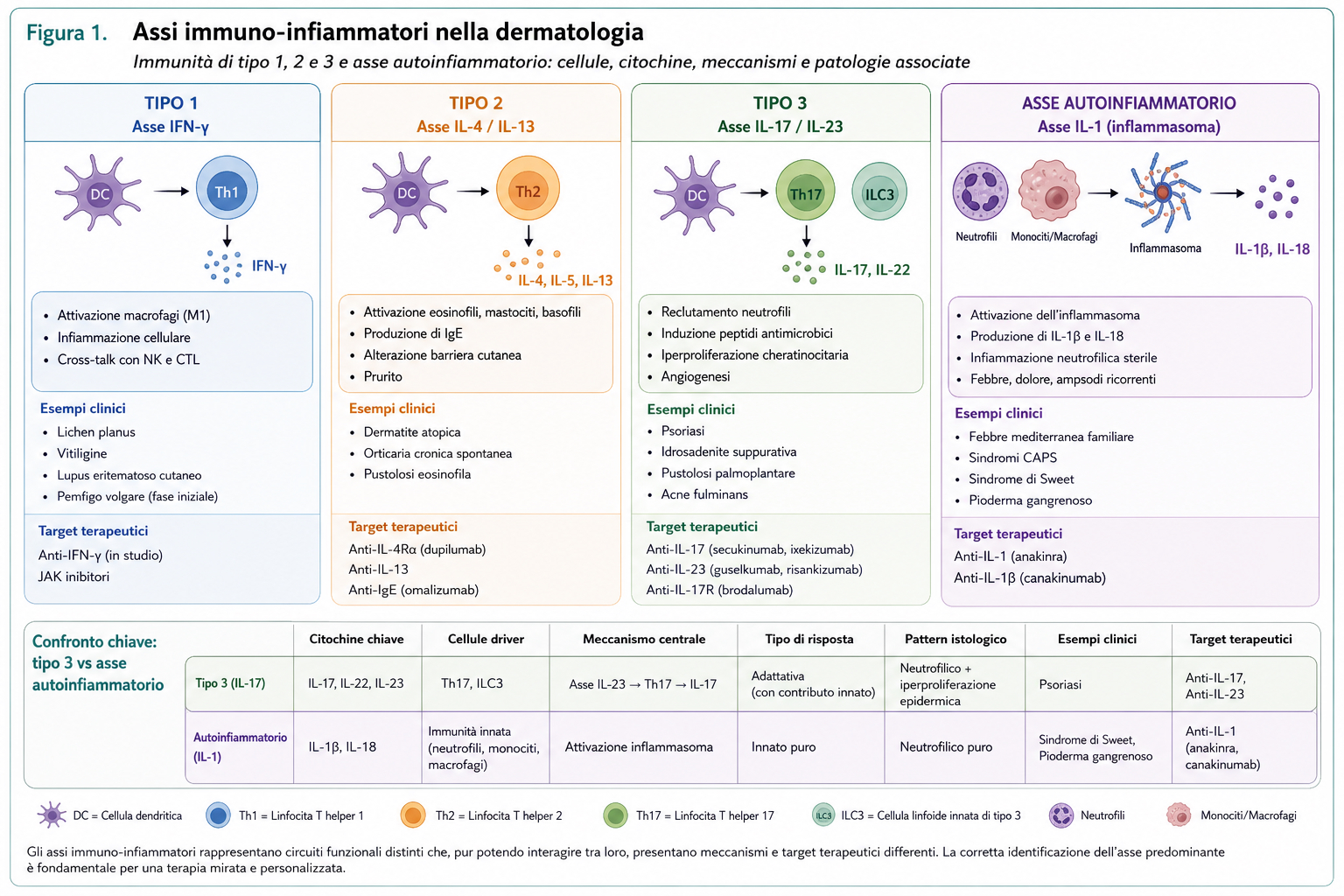
Schema riassuntivo degli assi immuno-infiammatori